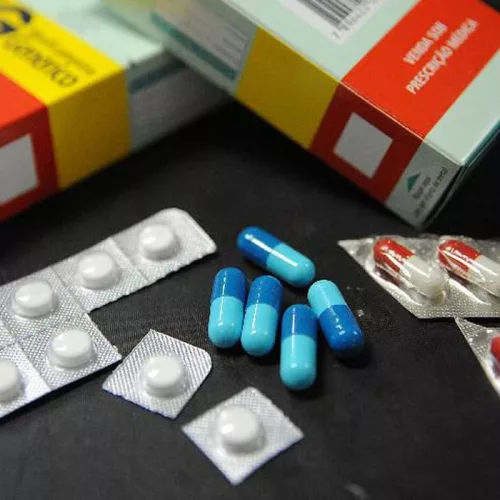
A Anvisa (Agência Nacional de Vigilância Sanitária) determinou, nesta quinta-feira (23), o recolhimento de lotes do medicamento losartana, que é um anti-hipertensivo e um dos remédios para insuficiência cardíaca mais utilizado no Brasil. Segundo a Anvisa, a decisão foi tomada em razão da presença da impureza “azido” em concentração acima do limite de segurança aceitável. Leia o posicionamento das empresas citadas e o que fazer se você comprou losartana dos lotes que devem ser recolhidos.
O prazo máximo regulamentar para conclusão do recolhimento dos produtos das farmácias é de até 120 dias, contados a partir de hoje, data da publicação da resolução, para a qual a Anvisa avaliou o impacto no mercado brasileiro e a necessidade de continuidade dos tratamentos.
A Anvisa orienta que pessoas que utilizam o remédio não devem interromper o seu tratamento. A hipertensão e insuficiência cardíaca exigem acompanhamento constante. Em caso de dúvida ou se precisar de orientação, o paciente deve conversar seu médico. “Deixar de tomar o remédio pode trazer riscos para a saúde”, alertou a Anvisa.
Os laboratórios que tiveram lotes com recolhimento determinado são PRATI DONADUZZI & CIA LTDA, CIMED INDUSTRIA S.A, BIOLAB SANUS FARMACÊUTICA LTDA (leia posicionamento da empresa), Aché Laboratórios Farmacêuticos S.A, LABORATÓRIO TEUTO BRASILEIRO S/A, BRAINFARMA INDÚSTRIA QUÍMICA E FARMACÊUTICA S.A, GEOLAB INDÚSTRIA FARMACÊUTICA S/A e EUROFARMA LABORATÓRIOS S.A.
Os lotes afetados estão descritos, um a um, no Diário Oficial da União. São duas resoluções, a 2.031, que congrega quase a totalidade de lotes atingidos e a 2.032, que afeta lotes da Geolab. A lista também pode ser conferida através do site da Anvisa.
Medida preventiva
Conforme a Anvisa, a medida preventiva foi adotada após a evolução do conhecimento sobre as impurezas e ela serve para adequar os produtos usados no Brasil aos limites técnicos previstos para a presença deste contaminante.
Por meio de nota, a Anvisa esclareceu que, desde a descoberta da possibilidade de presença do “azido” na losartana, em setembro de 2021, vem adotando medidas para garantir que os medicamentos disponíveis para a população brasileira estejam dentro dos padrões de qualidade.
A Anvisa disse que notificou os detentores de registro desses remédios para apresentarem os resultados da avaliação sobre a existência dessa impureza em seus produtos.
O que dizem as empresas citadas
Biolab Farmacêutica
NOTA DE ESCLARECIMENTO BIOLAB FARMACÊUTICA
Recolhimento preventivo de medicamentos com o princípio ativo Losartana
A Biolab Farmacêutica informa que está cumprindo a medida preventiva determinada pela Resolução-RE 2.031, de 22.06.2022, da Agência Nacional de Vigilância Sanitária (Anvisa), de recolhimento e suspensão da comercialização e distribuição de alguns lotes dos seus medicamentos que contenham losartana potássica.
A empresa comunica que os lotes disponíveis no mercado que não constam na resolução estão dentro dos novos limites preconizados pela Agência reguladora. A Biolab enfatiza que não haverá ruptura no fornecimento de seus produtos, não afetando a prescrição médica, o tratamento e controle da hipertensão dos pacientes.
A Anvisa esclarece que losartana é um medicamento seguro e eficaz para o tratamento de hipertensão e insuficiência cardíaca. “Não há risco imediato em relação ao uso dessa medicação”, como consta na publicação da Anvisa.
Adicionalmente, a própria Anvisa recomenda que os pacientes continuem tomando o medicamento, pois “a interrupção do tratamento da hipertensão arterial e da insuficiência cardíaca pode produzir malefícios instantâneos”, e conversem com seus médicos em caso de dúvida ou necessidade de orientação.
A Biolab deixa o canal do SAC 0800-724-6522 para informações adicionais. E reforça o compromisso com os mais altos padrões de qualidade, mantendo a eficácia e segurança dos seus medicamentos colocados à disposição da população brasileira.
São Paulo, 23 de junho de 2022
Atenciosamente,
Biolab Sanus Farmacêutica Ltda.